Dossier n°6, juin 2002
L'interféron bêta : Protéine phare contre la sclérose en plaques
par Pascal Chanson
![[ L'interféron bêta : Protéine phare contre la sclérose en plaques ]](/prolune/images/prolune_cover006.jpg)
Serono, une grande entreprise de biotechnologie basée à Genève, commercialise depuis quelques années un médicament contre la sclérose en plaques (SP) appelé Rebif. Ce dernier est distribué dans 72 pays, mais sa vente aux Etats-Unis était bloquée jusqu'au 8 mars dernier par une loi sur les médicaments orphelins. En effet, la Food and Drug Administration (FDA) - l'autorité qui légifère la mise sur le marché américain de tout nouveau médicament - avait garanti jusqu'en 2003 l'exclusivité du marché à la société Biogen qui a développé un médicament similaire du nom d'Avonex. Pour récupérer un marché américain au potentiel d'un milliard de dollars par an, Serono a réussi par des voies juridiques à contourner cette loi. Au cœur de cette bataille qui opposait deux géants de la biotechnologie, se trouve une fois encore une protéine : l'interféron bêta. [PDF] [english]
La sclérose en plaques grignote la myéline
![[ Dr Jean-Martin Charcot (1825-1893) ]](/prolune/images/prolune0206_2.jpg)
Fig.1 Dr Jean-Martin Charcot (1825-1893)
Décrite pour la première fois en 1868 par Jean-Martin Charcot (1825-1893), l'un des fondateurs de la neurologie clinique, la SP est une maladie chronique qui se déclare chez les jeunes adultes (20-30 ans) et touche pratiquement deux fois plus de femmes que d'hommes. En Suisse, près de 10'000 personnes souffrent actuellement de cette maladie.
Des troubles de l'équilibre et de la vue, des difficultés d'élocution, une grande fatigue et parfois même la paralysie sont les principaux symptômes, derrière lesquels se cachent une atteinte du nerf optique et du système nerveux central . Ces derniers sont constitués d'une multitude de " neurones ", c'est-à-dire des cellules nerveuses dont la forme est assez particulière : un "corps" qui ressemble un peu à une étoile avec un long prolongement appelé "axone" (voir figure 2) qui permet de relier un neurone à un autre neurone et ainsi de suite jusqu'à former un véritable réseau. D'ailleurs, on peut comparer cet ensemble à un réseau électrique extrêmement complexe ou les axones seraient les fils de connexion entre les différentes unités. Chaque axone est entouré d'une sorte de gaine appelée la " myéline" (voir encadré) qui sert d'isolant et permet d'accélérer l'influx nerveux le long des axones à la manière du plastique qui entoure les câbles électriques. Dans la SP, cette gaine est littéralement "grignotée", l'évolution de la maladie provoquant des trous de tailles variables pouvant atteindre jusqu'à quelques centimètres. Résultat : une perturbation de la transmission nerveuse qui se manifestent par des troubles moteurs, optiques et de la sensibilité. Aujourd'hui, on pense que la SP est une maladie auto-immune (voir plus bas) qui affecte le système nerveux central.
Copyleft
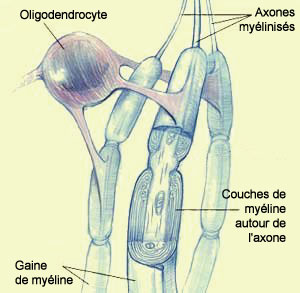
Fig.2 Transmission nerveuse à plus de 400km/h !
Dans le système nerveux central, la gaine de myéline est constituée de cellules appelées "oligodendrocytes". Ces dernières s'enroulent autour des axones et permettent, par leur propriété isolante, une transmission plus rapide de l'influx nerveux, pouvant atteindre 120 mètres à la seconde (432km/h).
Qu'est-ce qu'une maladie auto-immune ?
Lorsqu'un corps étranger (une bactérie, un virus etc.) pénètre dans notre organisme, ce dernier met en marche un système de défense, ou "système immunitaire", pour le combattre. Le système immunitaire doit éliminer " l'intrus " sans pour autant détruire son propre organisme. Dans une maladie auto-immune c'est pourtant ce qui se produit : le système immunitaire se dérègle et attaque une partie de notre corps. Dans les cas de SP, c'est la gaine de myéline des axones qui est visée. Cependant, les facteurs exacts qui déclenchent ce genre de maladie restent pour l'instant inconnus. Une prédisposition génétique, un virus qui agirait comme détonateur sont autant de pistes qu'explorent actuellement les chercheurs.
L'interféron gamma, le vrai coupable ?
Face à une infection, la " riposte " de notre système immunitaire peut prendre différentes formes (voir encadré). Une des voies de réponse rapide est la production d'interférons dont le rôle est justement " d'interférer " avec l'infection, c'est-à-dire de la ralentir jusqu'à ce que notre corps produise les anticorps nécessaires pour lutter contre l'intrus. Ces protéines furent identifiées en 1957 par deux virologues, le britannique Alick Isaacs et le suisse Jean Lindenmann, qui les ont réparties en trois classes selon leur taille et leur forme : alpha, bêta et gamma.
Les réponses du système immunitaire
La reconnaissance du "soi ", telle est la stratégie du système immunitaire. En effet, celui-ci a appris au cours de son développement à faire la différence entre " l'envahisseur étranger" et les constituants de son propre organisme, c'est à dire à distinguer le "soi " du "non-soi". Une fois, l'intrus identifié (un virus, une bactérie etc.), le système immunitaire peut employer plusieurs tactiques de défense. L'une d'entre elles est la production d'anticorps, c'est-à-dire des protéines en forme de Y qui iront s'attacher au corps étranger à la manière de fanions signalant ainsi sa présence à des cellules " nettoyeuses" (les macrophages) qui viendront l'exterminer. Une autre riposte possible est assurée par des cellules "tueuses" (les cellules cytotoxiques ou CTL). Si l'intrus a infecté des cellules du corps, les CTL reconnaîtront et détruiront ces cellules. D'autres cellules (les lymphocytes T auxiliaires) sont capables, après avoir détecté l'intrus, "d'activer" toutes les réponses du système. Finalement, en complément à cette solide stratégie de défense, vient s'ajouter une dernière ligne de "soldats" : les interférons. Leur rôle est de " ralentir " la prolifération de l'infection en attendant le renfort du système immunitaire.
Mais comment ces protéines interfèrent-elles avec l'infection ? Par exemple, lorsqu'une de nos cellules est infectée par des virus, elle fabrique des interférons de type alpha et bêta qui vont agir sur les cellules voisines. En réponse à cette action, ces dernières vont enclencher un mécanisme qui va les rendre plus "résistantes" à l'infection virale. D'autres interférons de type gamma - également produits par la cellule infectée - auront plutôt un rôle de "chef d'orchestre" : c'est-à-dire qu'ils moduleront d'autres voies du système de défense, comme par exemple la stimulation des cellules nettoyeuses (voir encadré).
Or plusieurs cas de SP laissent penser que c'est justement l'interféron gamma qui serait à l'origine de la maladie. En effet, il semble que l'identification de la myéline comme étant une "intruse" entraîne une surproduction d'interféron gamma. En plus de sa propre toxicité pour l'organisme, l'interféron gamma déclenche une cascade de réactions qui aboutira entre autres à la fabrication excessive de cellules dites "tueuses" (voir encadré). Normalement chargées de détruire les cellules "malades" (c'est-à-dire cancéreuses ou infectées par un virus ou une bactérie), les cellules tueuses se tromperaient alors de cible et détruiraient les cellules de la gaine de myéline.
L'interféron bêta, à la rescousse
Si l'on ne sait toujours pas pourquoi les maladies auto-immunes se déclarent, on sait pourtant comment ralentir leur progression. En effet, certains médicaments permettent de modifier (immunomodulateurs) et d'autres de carrément bloquer (immunosuppresseurs) les réactions du système immunitaire. Dans le traitement de la SP, l'interféron bêta lui-même constitue un médicament à effet immunosuppresseur. Grâce à différents procédés biotechnologiques, plusieurs types d'interférons bêtas ont pu être produits à des fins thérapeutiques. C'est l'interféron bêta 1b (produit dans des bactéries) qui fut le premier commercialisé sous le nom de Betaferon par la société Schering. Sa structure est légèrement différente de la forme naturelle car deux acides aminés diffèrent. L'interféron bêta 1a (fabriqué dans des cellules de mammifère) est quant à lui 100% identique à la protéine naturelle. Actuellement, deux sociétés le commercialisent sous deux noms différents. Serono propose le Rebif et Biogen l'Avonex, d'où la bataille qui opposait outre-atlantique ces deux monstres de la biotechnologie.
Pourtant le mécanisme d'action " thérapeutique" de l'interféron bêta est encore mal compris. Il semble que celui-ci agisse sur plusieurs molécules qui vont engendrer une cascade de réactions aboutissant finalement à la diminution de la concentration de l'interféron gamma. En agissant ainsi de façon indirecte, l'interféron bêta rétablirait un certain équilibre dans le système immunitaire (voir figure 3).
![[ Schéma d'un neurone ]](/prolune/images/prolune0206_4.jpg)
Fig.3 Schéma d'un neurone
A : Les cellules "tueuses" (CTL) du système immunitaire identifient la myéline comme " intrus", ce qui provoque une attaque de leur part qui vient s'ajouter à celle de l'interféron gamma.
B : L'interféron bêta diminue indirectement l'action de l'interféron gamma et des CTL.
La recherche continue
Si les médicaments à base d'interférons bêta ralentissent avec efficacité l'évolution de la SP, ils ne permettent pas de la guérir. C'est pourquoi, les scientifiques cherchent actuellement une molécule qui agisse de manière plus directe sur l'interféron gamma. Mais, comme vous l'aurez certainement ressenti au travers de ces quelques lignes, la complexité de notre système immunitaire rend cette tâche bien ardue !


