Dossier n°16, décembre 2005
Alzheimer : quand la personnalité s'égare
par Séverine Altairac
![[ Alzheimer : quand la personnalité s'égare ]](/prolune/images/prolune_cover016.jpg)
Forme de démence la plus fréquente chez les personnes âgées, la maladie d'Alzheimer a de quoi dérouter la communauté scientifique. Et pour cause. Son origine demeure une inconnue. Si on peut actuellement amoindrir certains symptômes, on ne peut encore enrayer le développement de la maladie. Il se pourrait bien que prochainement l'on assiste à de nouvelles avancées thérapeutiques. Les différents médicaments disponibles semblent être dirigés contre une seule et même cible : les protéines. La protéine amyloïde-β occupe certes le devant de la scène, pourtant elle est loin d'être la seule responsable du scénario fatal de la maladie d'Alzheimer. [PDF] [english]
18 millions de personnes. C'est le nombre de patients atteints d'une forme de démence de par le monde. Ces pathologies sont définies d'après l'Organisation Mondiale de la Santé comme l'altération progressive de la mémoire, du raisonnement et de la personnalité. Les démences dites séniles surgissent à un âge avancé et revêtent de nombreuses formes. Celle responsable de plus de la moitié des cas est la maladie d'Alzheimer (MA). En Suisse, on compte actuellement près de 90'000 patients atteints de la MA ou d'une autre forme de démence. En Europe, le risque touche plus de 5% de la population âgée de 70 à 74 ans et dépasse les 20% chez les plus de 85 ans. Aux Etats-Unis, environ 5% des personnes entre 65 et 74 ans développent la MA et près de 1 personne sur 2 en est atteinte au-delà de ses 85 ans. Malheureusement cela n'est qu'un début. Selon les experts, 34 millions de personnes développant cette pathologie ou une autre démence seraient à prévoir en 2025. Cette projection est indissociable d'un constat tout aussi vertigineux : dans nos pays riches et industrialisés, la population vieillit inexorablement. D'après le Fonds des Nations Unies pour la Population, ce phénomène s'étendra au monde entier avec un doublement de la proportion des plus de 65 ans d'ici 2050.
Dissolution de la personnalité
La MA peut se présenter sous deux formes. La première, très largement majoritaire, touche au hasard dans la population des personnes en général au-delà de leurs 70 ans. La seconde est héréditaire et beaucoup plus rare. Cette forme dite "familiale" se déclare plus précocement, en moyenne aux alentours de la quarantaine et au plus tôt vers les 30 ans. Sur l'ensemble des patients Alzheimer, les cas familiaux n'en représenteraient qu'à peine 5%.
Bien souvent et surtout dans les cas non héréditaires, il est difficile de diagnostiquer et dater un début de MA puisque les symptômes précoces se confondent avec les premiers signes du vieillissement cérébral normal.
Tout commence par de petits trébuchements de la mémoire. Des oublis bénins qui entravent la réalisation de tâches domestiques, des mots simples qui échappent. Les souvenirs récents ne trouvent plus de prise dans la mémoire. Qu'avez-vous mangé hier soir ? La question restera sans réponse exacte. En revanche les souvenirs anciens seront bien plus longtemps préservés.
Mais la mémoire n'est pas la seule faculté cognitive affectée. La concentration et l'attention faiblissent insidieusement : il devient de plus en plus pénible de suivre une conversation avec plusieurs personnes. Le langage s'appauvrit. A ces difficultés s'ajoutent des troubles de l'organisation de la pensée, du jugement et d'orientation dans l'espace et le temps. Progressivement les patients perdent la capacité à reconnaître les objets et les visages familiers deviennent anonymes. Graduellement leur autonomie quotidienne s'éteint jusqu'à ne plus pouvoir réaliser des gestes aussi simples qu'allumer une bougie et exécuter des tâches familières comme s'alimenter ou s'habiller.
Les patients présentent également un tableau de symptômes non-cognitifs douloureux à vivre pour leurs proches. Dès le début le la maladie, il est très fréquent qu'ils se laissent envahir par l'apathie, c'est-à-dire un manque d'intérêt et de motivation, et une perte des initiatives. Devenant associables, souvent irritables, angoissés, dépressifs ou agités, parfois en proie à des hallucinations, leur comportement et finalement leur personnalité sont profondément altérés. Après s'être installée pas à pas, la maladie poursuit son évolution sur une durée moyenne de 8 à 12 ans. Actuellement, il n'existe aucune thérapie curative et les patients succombent en général à des complications, comme la dénutrition ou la thrombose veineuse liée à la perte de mobilité.
Une maladie, une multitude de protéines
Fig.1 Aloïs Alzheimer (1864-1915)
C'est l'autopsie de la patiente Auguste D. en 1906 qui lèvera le voile sur cette pathologie dévastatrice. Le neuropsychiatre allemand Aloïs Alzheimer la suivra de 1901 à 1906 et recueillera les premières descriptions cliniques de la démence qui allait porter son nom. A la mort de sa patiente, Aloïs Alzheimer pratiqua l'examen de son cerveau. Il en observa une atrophie, que l'on montrera plus tard liée à une mort importante des cellules nerveuses, et identifia les deux types de lésions caractéristiques de ce qu'on allait nommer la maladie d'Alzheimer : les plaques séniles et les dégénérescences neurofibrillaires. Les plaques séniles apparaissent sous la forme de "pastilles" de protéines agrégées entre les cellules du cerveau tandis que les dégénérescences neurofibrillaires sont identifiables grâce à la présence de "cordelettes" de protéines à l'intérieur des neurones.
L'apparition de ces lésions succède à l'action de nombreuses protéines et la découverte de cas héréditaires de la MA a particulièrement attiré l'attention des scientifiques sur trois d'entre elles. Ce sont la protéine amyloïde et les présénilines 1 et 2. Les gènes qui contiennent la recette de fabrication de ces protéines peuvent porter des anomalies, appelées aussi mutations. Ces anomalies peuvent se transmettre de génération en génération et le porteur d'une mutation sur un de ces trois gènes n'échappera malheureusement pas à la maladie. Par conséquent il s'imposait de se pencher sur l'implication de ces protéines dans le déroulement de la MA.
Zoom sur la plaque sénile
La protéine amyloïde et les présénilines occupent une place centrale dans l'apparition des plaques séniles. Cette lésion typique de toutes les formes de la MA résulte de l'accumulation excessive entre les cellules d'un élément-clé : le fragment amyloïde-β (Aβ). Ce dernier est en réalité une protéine raccourcie dérivée de la protéine amyloïde. La protéine amyloïde, dont le rôle n'est pas encore bien défini, est localisée dans différentes cellules de l'organisme et en particulier dans la membrane des neurones.
Comment le fragment Aβ est-il alors libéré dans le cerveau ? La protéine amyloïde est systématiquement scindée en plusieurs fragments qui sembleraient offrir une protection aux neurones. Cette fragmentation est justement supervisée par les présénilines, entre autres. Un des fragments amyloïdes est en revanche toxique et a la propriété de changer de forme pour acquérir une structure plissée nommée "feuillet β". Il devient ainsi l'amyloïde-β. Ce fragment insoluble et "indestructible" est propice à l'initiation d'amas qui vont constituer le cœur des plaques séniles.
Les dépôts d'amyloïdes-β semblent exercer des méfaits multiples sur les neurones et il ne fait pas de doute que ces dépôts mettent progressivement leur vie en péril. Pour y faire face, le cerveau met en place une stratégie de défense, orchestrée par le système immunitaire qui délègue des cellules dans les plaques où elles tentent vraisemblablement de détruire les fragments Aβ. Mais le revers de la médaille est qu'elles contribuent à la production de radicaux libres, nocifs pour la survie neuronale, et amplifient ainsi l'effet toxique des plaques.
![[ Les lésions de la maladie d'Alzheimer.]](/prolune/images/prolune1205_2.jpg)
Fig.2 Les lésions de la maladie d'Alzheimer. Les dégénérescences neurofibrillaires se caractérisent par des "cordelettes" de protéines tau à l'intérieur des neurones, et les plaques séniles par des dépôts d'amyloïdes-β qui apparaissent sous la forme de "pastilles" situées entre les cellules.
Des cordelettes de protéines
La perte des neurones au cours de la MA est probablement due essentiellement aux dégénérescences neurofibrillaires (DN). A l'opposé des plaques séniles qui s'organisent à l'extérieur des cellules neuronales, les DN opèrent dans les neurones. La protéine tau est à la source de ces perturbations internes. Son rôle normal est étroitement associé à celui d'un ensemble de cylindres protéiques, les microtubules, dont elle facilite l'assemblage. L'architecture de ces microtubules contribue à la forme de la cellule tout comme les os dessinent le squelette. Ce sont aussi des voies de transport de nutriments et autres molécules à l'intérieur de la cellule. Tout chavire si, pour une cause encore non clairement déterminée, la protéine tau devient défectueuse. Elle perd alors toute affinité pour les microtubules qui dès lors se désagrègent. Résultat, la cellule se déforme. Les protéines tau anormales vont de surcroît s'agglutiner les unes aux autres sous l'aspect de "cordelettes" et signer ainsi l'apparence typique de ces lésions. Mais ce n'est pas tout. La dissolution des microtubules signifie également la perte des voies de transport vers les prolongements cellulaires des neurones - l'axone et les dendrites, organes de la communication nerveuse. Les neurones fonctionnent mal et finissent par mourir.
La mémoire en réseau
Deux types de neurones sont particulièrement fragilisés dans les lésions de la MA : les neurones glutamatergiques et les neurones cholinergiques. Le glutamate et l'acétylcholine, à l'origine du nom de ces neurones, sont de petites molécules indispensables à la communication nerveuse : les neurotransmetteurs. L'information circule d'un neurone à l'autre en franchissant des points de contacts, les synapses. Le neurone en amont de la synapse véhicule le message nerveux le long de son axone. Au niveau de la synapse, il libère des neurotransmetteurs pour transférer l'information vers le neurone suivant. Ce dernier va alors capturer les neurotransmetteurs via des récepteurs logés à la surface de ses dendrites. S'ensuivra la propagation du message nerveux le long de ce neurone vers la prochaine synapse. Un neurone n'est pas connecté à un seul autre mais à un très grand nombre et ensemble ils forment des réseaux.
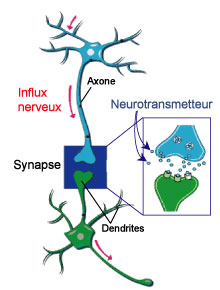
Fig.3 Composition d'une synapse. L'influx nerveux passe d'un neurone à l'autre grâce à la libération de neurotransmetteurs dans la jonction synaptique.
Dans le cortex et l'hippocampe, différentes zones relatives aux processus d'apprentissage et de mémoire (facultés cognitives cibles de la MA) abritent des neurones cholinergiques et glutamatergiques. Savons-nous où est élaborée la mémoire ? Au cœur des réseaux de neurones, semble-t-il. Comme une pâte à modeler, ces constructions neuronales s'adaptent pour conserver une empreinte des informations qui nous parviennent. Comment ? Les synapses sont modifiées pour que la transmission du message via les neurotransmetteurs devienne plus efficace. C'est ce que l'on nomme la plasticité synaptique. Le fragment Aβ à l'origine des plaques séniles pourrait bien agir à l'encontre de cet élégant mécanisme. Une récente étude a en effet montré que le fragment réduit la quantité d'un type de récepteurs au glutamate à la surface des neurones, ce qui affaiblirait la qualité de la transmission nerveuse.
L'étiolement des neurones au glutamate et à l'acétylcholine justifie l'emploi de certains médicaments. Les plus fréquents à l'heure actuelle sont l'Exelon, l'Aricept et le Reminil. Ils augmentent la durée d'action de l'acétylcholine dans l'espace synaptique en inhibant sa dégradation, ce qui permet de compenser le déficit cholinergique et améliorer la performance de mémoire. La Mémantine, une autre substance, agit sur un type de récepteurs glutamatergiques. Ces derniers, dans les conditions pathologiques de la MA, peuvent déclencher une cascade intracellulaire toxique, probablement liée en partie au fragment Aβ. En bloquant transitoirement ces récepteurs, la Mémantine assure une protection des neurones et pallie les troubles cognitifs. Cela peut paraître incompatible avec l'observation précédente selon laquelle moins de ces récepteurs affecte la transmission nerveuse. Les effets bénéfiques sont pourtant bien là et cette apparente contradiction illustre à quel point les évènements cellulaires sont complexes. Quoiqu'il en soit, pour ces deux types de thérapies, il s'agit de traitements symptomatiques qui restent imparfaits et aux effets modestes. Etant donné les difficultés à poser un diagnostic précoce de la MA, ces médicaments ne sont prescrits en général qu'à un stade relativement avancé. Hélas, la MA suit un processus dégénératif inéluctable et ces médicaments n'offrent pas d'espoir lorsque les neurones sont détruits.
L'œuf ou la poule ?
Le délabrement neuronal évolue de proche en proche dans les lésions de la MA. Concernant les dégénérescences neurofibrillaires, il a été établi qu'elles progressaient selon un certain parcours. Elles prennent naissance dans les aires les plus vulnérables du cerveau, le cortex entorhinal et l'hippocampe, lieux de passage obligés pour la formation de nouveaux souvenirs. Rappelons à ce propos que les premiers symptômes cognitifs sont des troubles de la mémoire. Graduellement les lésions vont s'étendre à tout le cortex : elles envahissent l'isocortex, centre d'intégration des informations sensorielles, puis remontent vers les aires de réception des cinq sens et les aires motrices, où sont élaborés les ordres. Quant aux plaques séniles, elles apparaissent dans l'isocortex puis s'associent ultérieurement aux dégénérescences neurofibrillaires.
On pense depuis longtemps que les toutes premières lésions à se révéler sont les plaques séniles. Cette théorie dite de "la cascade amyloïde" défend que l'accumulation des fragments Aβ provoquerait les dégénérescences neurofibrillaires puis la mort neuronale. Cette hypothèse est soutenue par les cas familiaux de la MA où les mutations dans la protéine amyloïde ou dans les présénilines conduisent à une surproduction de l'Aβ. D'autre part, il se trouve que le gène de la protéine amyloïde/Aβ se situe sur le chromosome 21. De ce fait, une personne atteinte de la trisomie 21 -syndrome de Down- a par conséquent trois copies de ce gène. Ce n'est pas sans nous interpeller puisque à l'approche de la quarantaine, tous les trisomiques 21 développent la MA, observation qui alimente l'hypothèse de la cascade amyloïde.
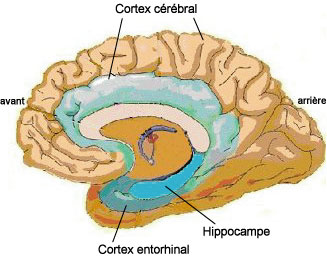
Fig.4 Régions cérébrales affectées par les lésions. Les dégénérescences neurofibrillaires progressent de l'hippocampe au cortex cérébral en passant par le cortex entorhinal ; les plaques séniles touchent l'ensemble du cortex cérébral.
Toutefois on peut noter que les plaques séniles ne sont pas la signature exclusive de la MA. Au cours du vieillissement cérébral normal, ces lésions surviennent également mais en quantité moindre certes, preuve que l'organisme peut tolérer les dépôts amyloïdes jusqu'à une certaine limite délicate à définir. Aujourd'hui la théorie de la cascade amyloïde est vivement controversée et se heurte essentiellement à deux observations. Nombre d'études ont souligné que, dans la majorité des cas, les dégénérescences neurofibrillaires précèdent les plaques séniles. De plus, la gravité des symptômes cliniques dépend de l'évolution des dégénérescences neurofibrillaires alors que sa relation avec les plaques séniles n'est pas fiable.
Finalement, qui de l'amyloïde-β ou de la protéine tau est la première à frapper ? Diverses hypothèses s'affrontent pour proposer un scénario qui réunit la formation des plaques séniles et l'apparition des dégénérescences neurofibrillaires. Lequel des deux événements précède, ou influence, l'autre? Progresseraient-ils conjointement ? Ont-ils un dénominateur commun ? Dans quel processus moléculaire ces deux lésions prennent-elles racine ? Autant de questions face à un seul problème : la cause de la maladie renferme encore bien des mystères à percer.
Echapper à la maladie
Si on a découvert des gènes dont les mutations sont responsables des formes précoces de la MA, existe-t-il des facteurs de risque ? Sans aucun doute, le facteur le plus puissant est l'âge. D'autre part, on a identifié des facteurs de prédisposition génétique dont le gène de l'apolipoprotéine E (Apo E). Cette protéine est bien connue pour son rôle dans le transport du cholestérol dans le sang. Il existe dans la population trois formes de ce gène (voir le glossaire, polymorphisme) . Sans pour autant être un facteur déterministe, la forme Apo E4 accroît de façon considérable le risque de la maladie. Il est estimé que 30 à 60 % des patients Alzheimer en sont porteurs. Comment Apo E4 agirait-elle ? Elle pourrait participer à la formation des dépôts amyloïdes et encouragerait ainsi le développement des plaques séniles.
N'oublions pas que les facteurs environnementaux tels que l'hypertension, le tabagisme, l'hypercholestérolémie, une alimentation pauvre en anti-oxydants, un traumatisme crânien favorisent probablement aussi la MA. Plusieurs études suggèreraient qu'un faible niveau d'éducation dans le jeune âge serait aussi un terrain propice au développement de la maladie. Par ailleurs, il semble que les oestrogènes ont un effet bénéfique sur le cerveau, la ménopause serait par conséquent un facteur de risque et exposerait davantage les femmes à la MA.
Vers une guérison ?
La maladie est très délicate à diagnostiquer et ce pour trois raisons essentiellement. Tout d'abord, les premiers signes ressemblent à s'y méprendre à ceux du vieillissement normal. Ensuite, les lésions cérébrales sont microscopiques et malheureusement uniquement décelables avec certitude par autopsie. Finalement il n'existe pas de molécules biologiques que l'on puisse détecter de manière fiable dans le sang ou dans le liquide céphalorachidien - liquide des méninges qui entoure le cerveau et la moelle épinière.
Quand les hésitations de la mémoire persistent et que la crainte de la MA s'installe, que faire ? Ce sont d'ailleurs bien souvent les proches qui s'inquiètent et redoutent une MA puisqu'en effet, les malades sous-estiment généralement leurs déficits cognitifs. Ils sont alors dirigés vers des "consultations mémoire" où ils seront soumis à une batterie de tests neuropsychologiques, qui vise à évaluer l'ensemble de leurs troubles cognitifs. Pour tenter d'affiner le diagnostic, des analyses en neuro-imagerie peuvent être envisagées : l'IRM (imagerie par résonance magnétique nucléaire) révèle l'atrophie de certaines aires cérébrales comme l'hippocampe dans la MA, et le SPECT (single photon emission computed tomography) mesure le flux sanguin cérébral témoin de l'activité du cerveau. Beaucoup d'espoirs reposent sur ce type de techniques qui pourraient relever le défi de la détection très précoce des lésions Alzheimer.
Si les inhibiteurs de la dégradation de l'acétylcholine et la Mémantine sont des traitements répandus, ils ne font que compenser temporairement une détérioration neuronale. Aujourd'hui les attentes se tournent vers la vaccination. Pourquoi ? Le principe de la vaccination est en effet de stimuler la production d'anticorps contre des protéines particulières. Pour ce faire, il suffit d'injecter dans l'organisme les protéines en question. L'idée ici est donc de "nettoyer" le trop plein de plaques séniles en induisant la fabrication d'anticorps contre le fragment Aβ. De premiers essais cliniques d'injection du fragment se sont déjà déroulés mais ont du être interrompus suite à des cas d'encéphalites. Sur l'initiative de la société Roche, une nouvelle vague d'essais sera lancée en 2006. Il s'agit cette fois d'injecter directement des anticorps anti-Aβ chez des patients Alzheimer, afin d'éviter une réponse inflammatoire. Par ailleurs, d'autres essais cliniques ont débuté l'automne dernier en Suisse et concernent le produit Alzhemed développé par la société Neurochem. Ce médicament agirait avant la formation des plaques séniles en bloquant directement l'agrégation des fragments Aβ.
Il existe de nombreuses autres pistes thérapeutiques basées sur des stratégies différentes et qui visent toutes à freiner l'évolution des lésions. Des espoirs pour les patients Alzheimer d'aller vers une guérison et de recouvrir l'intégrité de leur personnalité.


